关节炎症是困扰全球数亿人的常见健康问题,从晨起僵硬的膝关节到痛风发作时红肿的脚趾,这些症状背后都存在着复杂的生物学机制。在门诊室里,医生最常被问及的两个核心诉求是:"能否快速缓解疼痛"和"会不会损伤关节结构"。传统消炎药物虽然能暂时压制症状,却难以阻止关节软骨的持续磨损。令人振奋的是,新一代靶向药物通过双重作用机制,正在改写这一困局——像精准的纳米机器人般,既能关闭疼痛信号,又能启动组织修复程序。
一、疼痛信号的精准拦截:从广谱阻断到靶向调节
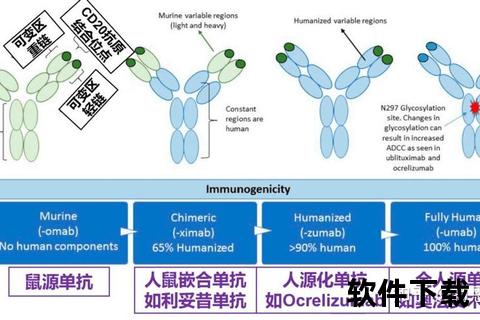
传统非甾体抗炎药(NSAIDs)通过抑制环氧合酶(COX)降低前列腺素水平,但这种"地毯式轰炸"可能误伤胃黏膜保护机制和心血管系统。新型COX-2高选择性抑制剂(如依托考昔)通过区分结构异构体,将抗炎作用集中在外周炎症部位,减少消化道出血风险。更前沿的趋化因子受体拮抗剂(如PF-06835375)能精准阻断免疫细胞向关节的迁移,从源头抑制炎症瀑布反应。
在疼痛传导通路上,钠离子通道Nav1.7成为关键靶点。临床研究显示,新型小分子抑制剂可使80%骨关节炎患者的疼痛评分下降50%,且不影响触觉感知。这种精准调控避免了类药物的成瘾风险,尤其适合需要长期用药的慢性患者。
二、组织修复的分子开关:从被动防御到主动重建
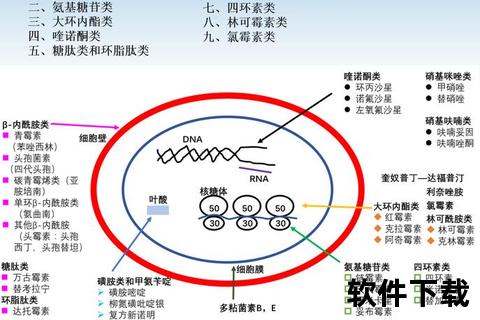
突破性进展在于药物同时具备抗炎和促修复功能。锝[99Tc]亚甲基二膦酸盐(云克)通过双重机制发挥作用:一方面抑制IL-1β、TNF-α等炎性因子,另一方面激活成骨细胞分化因子RUNX2,促进骨关节重塑。临床数据显示,持续使用3个月可使关节间隙狭窄进展减缓67%。
间充质干细胞(MSC)疗法开创了生物修复新纪元。这些"智能药物工厂"不仅分泌抗炎细胞因子,还能分化为软骨细胞填充缺损。2025年公布的502例临床试验证实,关节内注射干细胞可使WOMAC评分改善42%,且修复效果持续12个月以上。更令人惊叹的是,查尔酮衍生物通过调控RANKL/RANK/OPG系统,既能抑制破骨细胞活性,又能刺激软骨基质合成,在动物模型中展现出软骨厚度增加30%的效果。
三、个体化用药的智慧选择:从统一方案到精准匹配
面对琳琅满目的新药,临床决策需考虑三大维度:①炎症类型(机械性磨损vs自身免疫攻击);②组织破坏阶段(早期水肿vs晚期骨赘形成);③患者特征(肥胖人群需侧重脂肪因子调节,绝经女性需关注雌激素受体调控)。
以类风湿关节炎为例:ACPA阳性高风险人群可采用阿巴西普进行免疫干预,将疾病进展风险降低74%;而骨关节炎患者更适合联合使用P2X3受体拮抗剂(控制神经源性疼痛)和金属蛋白酶抑制剂(保护软骨基质)。特殊人群如孕妇,可考虑局部应用辣椒素贴剂,其通过耗竭P物质发挥镇痛作用,系统吸收量仅为口服药的1/200。
四、居家管理的科学策略:从被动治疗到主动防护
1. 疼痛日记记录法:用视觉模拟量表(VAS)每日三次记录关节疼痛、僵硬程度,配合手机APP分析症状波动规律,可提前1-2天预判急性发作。
2. 阶梯式冷热疗法:急性肿胀期采用冰敷(每次15分钟,间隔2小时)收缩血管;慢性期改用40℃石蜡浴促进修复因子渗透。
3. 靶向营养补充:最新研究证实,姜黄素纳米微粒与乳香酸联用,可增强抗炎效果3倍且不增加肝酶水平。
4. 智能护具辅助:压力传感膝关节支具能实时调整支撑力度,在上下楼梯时自动增加15%的稳定性。
五、就医时机的精准判断:从经验判断到量化标准
当出现以下预警信号时需立即就诊:①夜间痛醒超过3次/周;②关节活动范围减少>50%;③超声显示滑膜厚度≥4mm伴血流信号增多。最新的生物标记物检测可在结构破坏前6个月预警风险,包括血清COMP碎片升高和miRNA-140水平下降。
在药物选择上,短期急性期优先考虑起效时间<30分钟的洛索洛芬钠口服液,而长期管理推荐采用每月1次的抗NGF单抗注射,其持续镇痛效果可达传统药物的5倍。对于已经出现软骨下骨暴露的患者,关节腔注射交联透明质酸复合PRP可形成物理屏障,为干细胞治疗争取时间窗口。
这场静默的关节保卫战中,每个患者都是自身健康的第一责任人。当我们握紧靶向治疗这把"智能钥匙",不仅能打开疼痛枷锁,更能重启组织的自愈程序。从今天开始记录关节的"晴雨表",在专业医生指导下制定个性化方案,让每一次行走都成为修复之旅而非磨损之路。
