类风湿关节炎(RA)是一种以关节滑膜炎为主要特征的慢性自身免疫性疾病,其核心病理机制是免疫系统异常激活导致的关节破坏和全身炎症反应。随着靶向治疗的快速发展,生物制剂和JAK抑制剂已成为突破传统治疗瓶颈的关键手段。本文将从疾病机制、药物选择、临床决策和患者管理多角度展开分析,为患者和公众提供科学指导。

一、靶向治疗的核心机制:从“失控的免疫”到精准干预
RA的发病与多种免疫细胞异常活化相关,包括B细胞过度分泌自身抗体、T细胞异常增殖,以及巨噬细胞向促炎型M1极化等。这些细胞释放的炎症因子(如TNF-α、IL-6)形成“细胞因子风暴”,加速关节侵蚀。
生物制剂通过特异性阻断关键炎症因子发挥作用,例如:
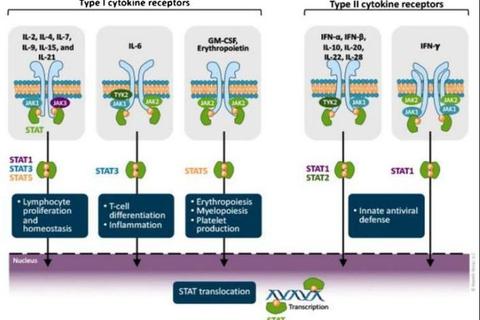
JAK抑制剂则通过细胞内信号调控实现更广泛的抗炎效果。JAK-STAT通路是多种细胞因子(如IL-2、IL-7、IFN-γ)的共同传导路径,托法替布等药物通过抑制JAK激酶活性,阻断下游炎症信号。与生物制剂相比,JAK抑制剂具有口服便利性,但需注意心血管和感染风险。
二、临床选择策略:个体化治疗的“四步决策法”
1. 基础治疗评估
甲氨蝶呤仍是RA治疗的基石,约50%患者单药治疗可实现低疾病活动度。若治疗3个月未达标,需考虑升级方案。
2. 靶向药物选择依据
| 患者特征 | 优先推荐方案 | 科学依据 |
|-|--||
| 合并肺纤维化 | IL-6抑制剂(如托珠单抗) | 抑制IL-6可减轻肺部炎症 |
| 反复感染史 | JAK抑制剂(如乌帕替尼) | 避免生物制剂的长期免疫抑制 |
| 难治性多关节肿胀 | 双靶点生物制剂(如泰它西普) | 同时阻断BLyS/APRIL通路提升疗效 |
| 合并心血管疾病 | 避免高剂量JAK抑制剂 | 降低血栓风险 |
3. 特殊人群管理要点
4. 疗效监测与调整
采用DAS28评分系统每3个月评估一次,若治疗6个月未达标,可尝试“生物制剂+JAK抑制剂”联合治疗。研究显示,IL-6抑制剂与托法替布联用可使ACR50应答率提升至68%。
三、前沿进展与未来方向
1. 双靶点药物突破:荣昌生物的泰它西普通过同时抑制BLyS/APRIL通路,在Ⅲ期试验中使79%患者实现ACR20缓解,较传统药物提升30%。
2. 细胞治疗曙光:CAR-T疗法在难治性RA中初显成效,3例患者接受CD19靶向治疗后,6个月内类风湿因子转阴,且无严重不良反应。
3. 精准预测模型:基于基因检测的JAK亚型分析(如JAK1高表达者更适用乌帕替尼)正在临床试验中,有望实现“一人一策”。
四、患者行动指南:从认知到实践的“五步管理”
1. 症状预警:晨僵超过30分钟、对称性关节肿痛需尽早就诊,早期干预可降低50%致残风险。
2. 居家护理:急性期用冷敷减轻肿胀(每次15分钟),慢性期用40℃热敷缓解僵硬。
3. 药物依从性:生物制剂漏注射需在3天内补用,JAK抑制剂需固定时间服用以维持血药浓度。
4. 感染防控:接种肺炎球菌疫苗后再启动生物制剂治疗,避免活疫苗接种。
5. 功能锻炼:推荐水中太极、抗阻训练,每日活动量以“次日无疲劳感”为度。
RA治疗已进入“靶向时代”,但药物选择需权衡疗效与安全性。建议患者每半年进行超声检查评估关节损伤,并与风湿免疫科医生共同制定动态治疗方案。未来随着基因编辑和人工智能预测模型的发展,RA有望从“可控”走向“根治”。
